第一作者:袁建华
通讯单位:同济大学
论文DOI:10.1021/acsmaterialslett.4c01360

研究背景
卤化铅(Pb)钙钛矿太阳能电池(PSCs)因其低成本、卓越的光电性能和高达26.1%的能量转换效率而成为一种新兴的光伏技术。然而,铅离子的毒性和环境稳定性问题阻碍了其广泛应用。作为无铅替代品,锡(Sn)基钙钛矿作为一种有前景的替代材料,提供了优异的光电特性,并且通常被认为毒性更低。然而,锡钙钛矿仍可能存在一定的生物毒性和环境危害。如Babayigit等人使用模式生物斑马鱼(Danio rerio)研究了PbI2和SnI2的环境效应。结果发现,暴露于SnI2的胚胎比暴露于PbI2的胚胎在相同浓度下具有更高的致死反应。此外,Rüdel等人总结了Sn(II)和Sn(IV)对浮游蓝藻生长的抑制作用。发现毒性随着锡浓度的增加而增加,其中Sn(II)的生物毒性高于Sn(IV)。
从钙钛矿吸光材料中泄漏的重金属离子(Mn+)在太阳能电池受到机械应力、极端天气或意外事件时,可能会发生泄漏,并对环境构成风险。这些离子的生物累积可能通过食物链对生物造成不可逆的伤害。泄漏的Pb(II)和Sn(II)的毒性突显了从环境中去除这些离子的关键必要性。研究已经探讨了在实验室条件下使用化学和生物方法去除Cu(II)、Pb(II)和Cd(II)等各种Mn+。然而,对PSCs中Mn+泄漏的关注有限,对从钙钛矿中去除Pb(II)和Sn(II)的环境自我清除机制的理解仍然不足。因此,开发有效的Mn+泄漏处理方案对于管理和减轻其环境风险至关重要。
本研究首次探讨了环境微生物对钙钛矿泄露Mn+的处理。利用在环境中大量存在的废酵母作为“过滤器”,有效处理从PSCs中泄漏的Pb(II)和Sn(II)。我们评估了酵母对Pb(II)和Sn(II)的吸附能力,并研究其固定机制。该研究从多个角度提供了对Pb(II)和Sn(II)微生物吸附和转化过程的见解。这种方法在低成本和无污染的钙钛矿重金属生物处理方面具有重大进展,消除了对化学螯合试剂的依赖,并最小化环境影响。
内容简介
金属卤化钙钛矿太阳能电池(PSCs)在新兴光伏技术中展现了日益增长的商业化潜力。然而,PSCs中如Pb(II)和Sn(II)等Mn+的潜在泄漏对环境和健康构成了重大威胁,而环境对这些威胁的应对能力仍然未知。本研究首次报告了环境自然修复在应对钙钛矿泄漏风险方面的潜力。结果发现,环境废酵母可以通过物理和化学吸附机制的结合有效捕获泄漏的Pb(II)和Sn(II)。这些钙钛矿重金属随后被生物转化并固定。此外,我们的研究显示,Sn离子的去除率更高,并揭示了采用无铅钙钛矿光伏材料的环境可持续性得到增强。本研究提出了一种微生物清除策略,用于去除环境中的钙钛矿泄露的Mn+,推动钙钛矿光伏技术的实际应用。
图文导读
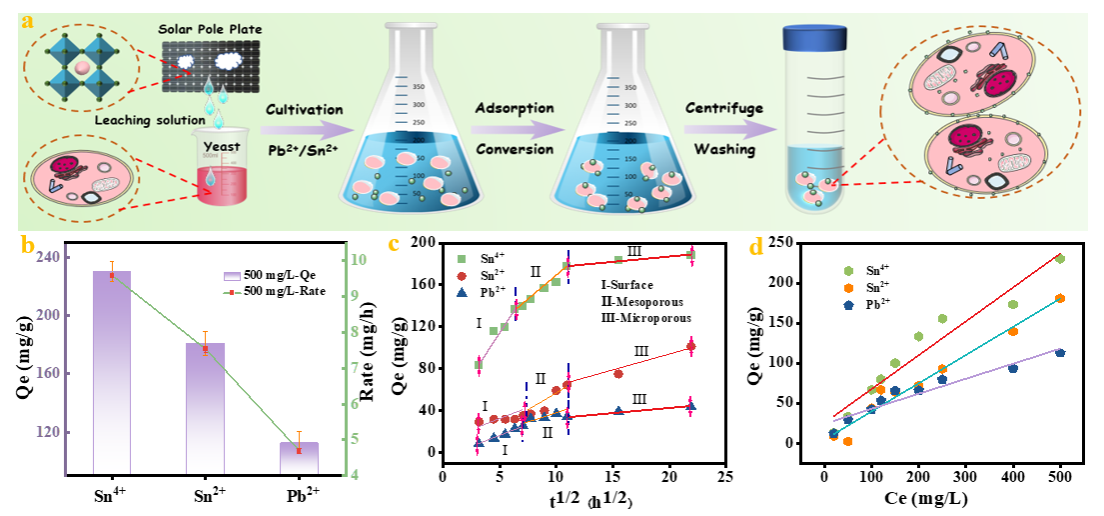
Figure1.Adsorption characteristics.(a) Theprocess of adsorption of theMn+by yeasts; Adsorption capacityat 500 mg/L Mn+concentration(b), adsorption kinetics (c), and adsorption isothermsat 20-500 mg/L Mn+concentrations(d).
为了探究环境暴露后微生物对卤化钙钛矿中Mn+的去除作用,我们模拟了Pb(II)、Sn(II)及其氧化态Sn(IV)的吸附过程,这些物质在空气暴露下可以迅速从Sn(II)转化而来,如图1a和S1所示。为了研究酵母对钙钛矿浸出液中Mn+去除的影响,我们探讨了酵母对MX2和MAMX3(M: Sn / Pb,X: I / Cl)的处理效果。图S2显示,作为A位阳离子的有机盐可以显著提高Mn+的去除效果(提高了1/3)。通过考察不同卤素在金属盐中的影响,我们发现氯基金属盐的去除效率几乎是碘基金属盐的两倍,因此随后用于评估不同Mn+对钙钛矿太阳能电池(PSCs)的环境影响。图1b中的吸附结果显示,酵母对不同物质的吸附能力存在显著差异,其中Sn(IV)的吸附能力最高,为230.3 mg/g,其次是Sn(II)的180.9 mg/g,Pb(II)为112.7 mg/g。与其他研究相比,活化酵母对Pb(II)的吸附表现更为出色。例如,Neil Gershenfeld培养的酵母在初始Pb浓度低于百万分之一的溶液中显示了12 mg/g的吸附能力,而其他微生物对Pb(II)的吸附能力通常在5到70 mg/g之间。这表明酵母对Sn离子的去除效果更为有利。吸附过程通过初级和次级动力学模型进行了拟合,如图S3a-c和表S1所示。根据R2值的比较,次级动力学模型的拟合效果最好,表明在吸附过程中酵母与Mn+之间存在化学吸附。同时观察到,在初始阶段,液膜扩散主导了酵母表面,这一点从高线性度中可以看出。随着过程的进展,线性度保持不变,表明吸附扩散到酵母内部。在后期,线性度的下降暗示了接近吸附平衡。此外,拟合的直线没有超过原点,提示存在其他过程,如表面吸附、液膜扩散、外部扩散,以及粒内扩散等。
为了分析酵母对不同Mn+的吸附特性,我们使用了三种典型的非线性吸附等温模型(Langmuir、Freundlich和D-R)以及Henry的线性模型。如图1d、图S3d-f和表S2所示,Langmuir和Freundlich模型均表现出对酵母吸附Mn+的优良拟合(R2> 0.907),这表明酵母表面存在具有不同能量和反应基团分布的异质吸附位点。吸附系数KF的排序为Pb(II) > Sn(II) > Sn(IV),这意味着细胞对Pb(II)的亲和力更强。吸附指数(1/n)值(范围从0.556到0.905)均小于1,表明酵母对Mn+的吸附效率较高,但随着Mn+浓度的增加,效率逐渐降低。这可能归因于酵母表面高能吸附位点的优先占据,影响了整体的吸附过程。Henry的线性模型结果表明,微塑料和污染物之间存在分配-扩散效应,其中Sn(IV)的吸附分配系数(Kp = 25.51 L/mg)显著高于Sn(II)(Kp = 4.524 L/mg)。这反映出酵母对Sn(IV)的吸附能力更强。总体而言,酵母对Mn+的吸附主要符合非线性拟合,这对应于物理和化学吸附过程的结合。

Figure 2.Structural information.SEM images and elemental mappings of pure yeasts (a-c), Sn(II)-adsorbed yeasts(d-f), Sn(IV)-adsorbed yeasts(g-i), and Pb(II)-adsorbed yeasts(j-l).
进一步研究了酵母在吸附Pb和Sn离子过程中结构的变化,分别通过扫描电子显微镜(SEM)和透射电子显微镜(TEM)观察了细胞内外的情况。对照组在超纯水中培养的酵母细胞表现出光滑的表面、完整的细胞壁和无异常(图2a-c和图S4a-b)。相比之下,Pb(II)吸附的酵母显示出严重的细胞壁破裂和脱离,伴随着细胞收缩和表面稀疏分布的颗粒(图2d-e),这表明Pb(II)具有更高的生物危害潜力。Sn(II)吸附的酵母表现出皱缩的表面和大量细小颗粒(图2g-h)。Sn(IV)吸附的酵母在表面显示出更多类似代谢产物的团块(图2j-k),这可能是其更高吸附能力的原因。TEM结果(图S6)揭示了Pb(II)吸附的酵母形成了含Pb的物质聚集体。空间映射(图2f、i、l和图S6d、h、l、p)和能量色散谱(EDS)证实了Sn(II)、Sn(IV)和Pb(II)的吸附和转化,形成了不同尺寸的小颗粒(图S5和图S7)。
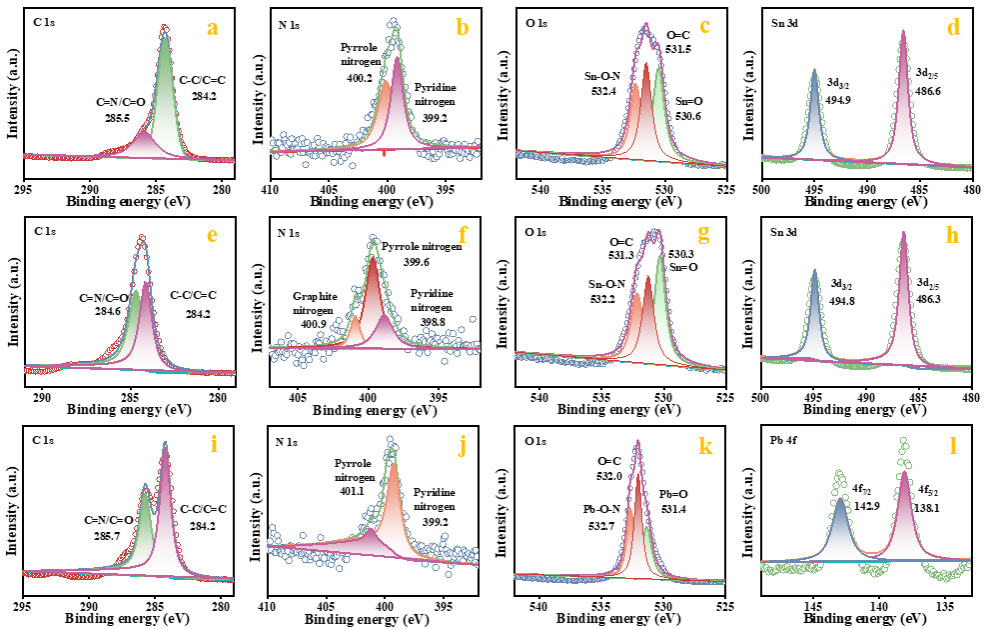
Figure 3.Capture and conversion of perovskite’s Mn+.XPS surface survey scan spectra of the samples.Sn(II)-adsorbed yeasts: (a) C 1s, (b) N 1s, (c) O 1s and (d) Sn 3d; Sn(Ⅳ)-adsorbed yeasts: (e) C 1s, (f) N 1s, (g) O 1s and (h) Sn 3d; Pb(II)-adsorbed yeasts: (i) C 1s, (j) N 1s, (k) O 1s and (l) Pb 4f.
为了探讨功能基团在酵母表面上的作用,使用X射线光电子能谱(XPS)分析了酵母在吸附前后表面的化学成分(图3,图S8a-c)。具体而言,我们检测了C 1s、O 1s、N 1s、Pb 4f和Sn 3d,以识别C、O、N与Mn+之间可能存在的化学键。拟合分析显示,C 1s峰可以分解为C=N/C=O(284.6-285.7 eV)和C-C/C=C(284.2 eV),而N 1s峰可以分解为吡啶氮、吡咯氮和石墨氮。O 1s峰对应于C=O、Sn=O/Pb=O以及Sn-O-N/Pb-O-N键。结果观察到,Mn+吸附后这些键的大小和形状发生了显著变化,表明酵母表面蛋白质和碳水化合物中的羧基、氨基、羟基和酰胺基团在Mn+的吸附中发挥了作用。Sn 3d和Pb 4f峰被分解为Sn 3d3/2(494.9 eV)、Sn 3d2/5(486.6 eV)、Pb 4f7/2(142.9 eV)和Pb 4f5/2(138.1 eV),这表明在酵母生物转化后存在Sn(IV)和Pb(IV)。此外,XRD结果表明,酵母对Sn(II)的吸附导致了Sn颗粒和SnO2的形成,而Pb(II)的吸附则导致了Pb3O4和少量PbO2的形成(图S8d)。从分析中可以看出,酵母细胞内的蛋白质、多糖和碳水化合物积极参与了Mn+的化学吸附过程(图S8e)。
傅里叶变换红外光谱仪(FTIR)被用来识别和分析酵母中的功能基团及其变化(图S8f)。分析显示,3293 cm-1和2922 cm-1的谱带主要来源于细胞中蛋白质和碳水化合物中的O-H和-NH2伸缩振动以及-CH2的非对称伸缩振动。1647 cm-1和1541 cm-1的谱带归因于酰胺I和酰胺II,其中酰胺I来源于C-O伸缩振动,酰胺II来源于N-H。1245 cm-1的谱带可能归因于酰胺III的存在,其具有混合的C-N和N-H振动峰。此外,1175到1150 cm-1的吸收带主要归因于酵母多糖中C-O键的伸缩振动。在Sn(II)和Pb(II)被酵母吸附后,616-650 cm-1范围内出现了Sn-O-Sn和Pb-O-Pb的光谱峰,表明氧原子参与了配位反应。这导致了O-H键长度的增加和振动峰的红移,而C=O和N-H则向更高波长移动,可能是由于Mn+与蛋白质相互作用引起的酰胺带振动峰的变化。Mn+吸附后位于550-750 cm-1的C=C完全吸收,表明可能与蛋白质形成了络合物。FTIR结果表明,在Mn+的化学吸附过程中,酵母细胞中的蛋白质、多糖和其他碳水化合物积极参与了这一过程。
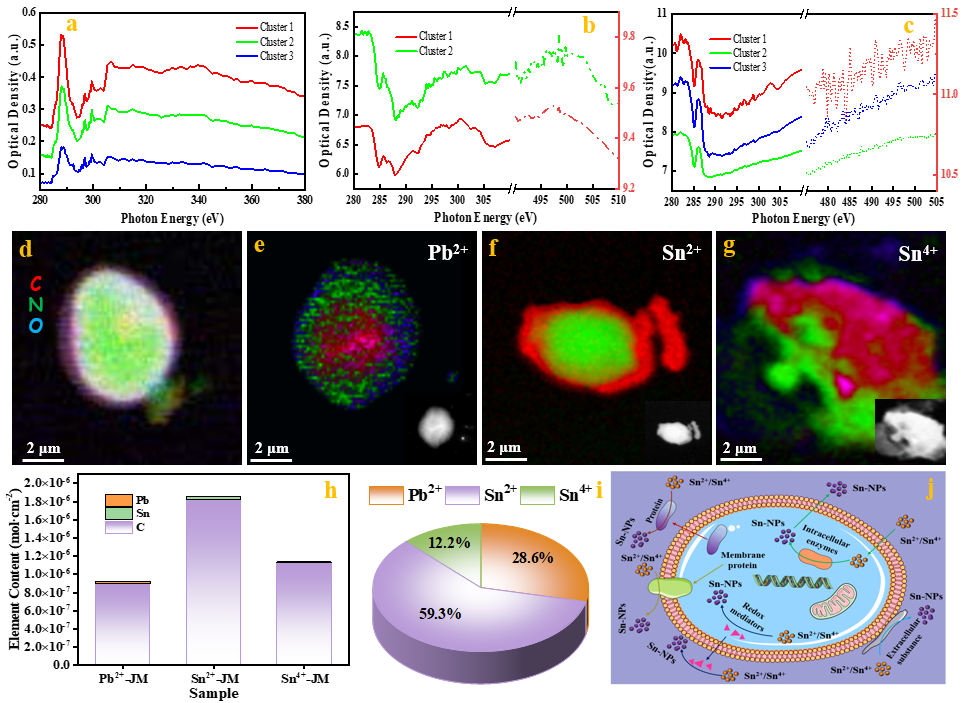
Figure 4.Quantitative analysis.XANES at C K-edge and metal M-edge extracted from different color regions in PCA analysis of the Pb(II)-adsorbed yeasts(a),Sn(II)-adsorbed yeastssamples (b), and Sn(IV)-adsorbed yeastssamples (c); PCA analysis of (d) pure yeasts, (e) Pb(II)-, (f) Sn(II)-, and (g) Sn(IV)-adsorbed yeasts; (h) Quantitative analysis of element concentration. Absolute content statistics of metal and C elements in each sample. (i) Quantitative element concentration. The pixel values represent the sample’s thickness. (j) Microbial adsorptions mechanism for perovskite’sSn(Ⅳ).
最后使用扫描透射X射线显微镜(STXM)确认了吸附了钙钛矿中重金属Mn+的酵母的电子结构和整体成分。来自碳K边缘和金属元素M边缘的STXM平均图像分别显示了酵母吸附Pb(II)、Sn(II)和Sn(IV)的情况(图4a、b和c)。像素值代表样品的厚度。主成分分析(PCA)显示出不同的化学成分簇(图4d、e、f和g),金属主要分布在酵母核心区域,表面金属含量较低(图S9)。我们根据酵母的碳含量对吸附的金属离子进行了归一化处理,可以明显发现,酵母吸附的Sn离子量高于Pb离子,其中Sn(II)的比例达到了59.3%,远高于Sn(IV)和Pb(II)(分别为28.6%和12.2%)。定量分析显示,酵母的Pb和Sn含量分别为0.0177 mol/cm⟡和0.0258 mol/cm⟡,突显了酵母对钙钛矿中Sn离子的更高吸附能力(图4h、i)。
此外,我们还假设了酵母吸附的机制,如图4j所示,酵母细胞对Pb(II)、Sn(II)和Sn(IV)的吸附过程可分为两个阶段。第1阶段是细胞表面吸附阶段,在此阶段,细胞壁上的细胞外聚合物和功能基团(如羧基、磷酸酰基、羟基、硫酸根和酰胺基团等)与Mn+发生配位络合。第2阶段是Mn+从细胞表面转移到细胞内部,并在细胞表面相关酶(如水解酶、转移酶等)的作用下参与细胞代谢的过程。根据实验结果分析,酵母的吸附机制主要包括表面络合、无机微沉淀和静电吸附。例如,SEM、TEM和STXM确认了Mn+不仅沉积在酵母表面,还进入了细胞内部,XRD、XPS和FTIR证实了生化转化过程的存在,同时Mn+与细胞表面形成了共价键,如Sn=O、Sn-O-N、Pb=O、Pb-O-N等。上述结果确认了酵母对Mn+的吸附不仅包括静电吸附,还包含化学吸附过程,同时也包括化学吸附和生物转化过程。
总结与展望
总之,本研究填补了钙钛矿太阳能电池(PSCs)与环境风险之间的知识空白。研究结论表明,通过作为生物吸附剂的环境酵母,可以管理来自PSCs的Pb(II)和Sn(II)的泄漏风险。尽管Mn+具有毒性,酵母表现出显著的耐受性,并实现了对Pb(II)和Sn(II)的高吸附容量,分别为112.7 mg/g和180.9 mg/g。该吸附过程以非线性Langmuir和Freundlich模型为特征,涉及物理和化学机制的结合。此外,酵母对Pb(II)和Sn(II)以及其氧化态Sn(IV)的吸附主要归因于蛋白质、多糖和其他碳水化合物功能基团。这些吸附的金属可以被生物转化为安全和稳定的金属氧化物。本研究不仅推进了对钙钛矿中重金属微生物吸收和转化的理解,还提出了一种实际的自我净化策略来管理PSCs生命周期中Mn+的泄漏。本研究认为,作为一种可持续解决方案,微生物与Mn+之间的联系将显著提升PSCs的环境安全性。
文献链接
https://doi.org/10.1021/acsmaterialslett.4c01360
另:封面图